2.2) Khi hòa tan m gam kim loại nhôm vào dung dịch HCl dư thấy V1 lít khí H2(đktc). Nếu cũng lấy m gam kim loại M tác dụng HCl dư thoát ra V2 lít H2(ĐKTC). Biết V1=3,06V2. Tìm kim loại M?
GIÚP T VỚI Ạ!!!
Hòa tan hết 8,1 gam kim loại M vào dung dịch HCl lấy dư thấy thu được 10,08 lít khí H2 (đktc). Nhận xét về kim loại M là đúng?
A. M tác dụng với dung dịch HCl và NaOH.
B. M là kim loại nặng.
C. M có độ dẫn điện lớn hơn so với Cu
D. M được điều chế bằng nhiệt luyện
Đáp án A
Gọi M có số oxi hóa từ 0 lên +n
BT e: ta có: 8,1n/ M = 10,08. 2/ 22,4
Tìm được M = 9n.
Cặp nghiệm thỏa mãn là n= 3 và M= 27 (Al)
+ Al có thể tác dụng với dd HCl và NaOH
+ Al được điều chế bằng phương pháp điện phân nóng chảy
+ Độ dẫn điện của Al < Cu
+ Al là kim loại nhẹ ( 2,7 g/ cm^3)
Hòa tan hết 8,1 gam kim loại M vào dung dịch HCl lấy dư thấy thu được 10,08 lít khí H2 (đktc). Nhận xét về kim loại M là đúng?
A. M tác dụng với dung dịch HCl và NaOH.
B. M là kim loại nặng.
C. M có độ dẫn điện lớn hơn so với Cu.
D. M được điều chế bằng nhiệt luyện
Đáp án A
Gọi M có số oxi hóa từ 0 lên +n
BT e: ta có: 8,1n/ M = 10,08. 2/ 22,4
Tìm được M = 9n.
Cặp nghiệm thỏa mãn là n= 3 và M= 27 (Al)
+ Al có thể tác dụng với dd HCl và NaOH
+ Al được điều chế bằng phương pháp điện phân nóng chảy
+ Độ dẫn điện của Al < Cu
+ Al là kim loại nhẹ ( 2,7 g/ cm^3)
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít khí H2 đktc. Kim loại M là kim loại nào sau đây?
A. Fe.
B. Al.
C. Ca.
D. Mg.
Đáp án B.
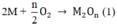
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
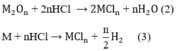
Số mol H2: 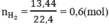
Theo phương trình (1)
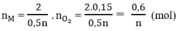
Theo phương trình (3)
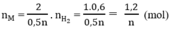
Tổng số mol M là 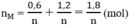
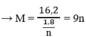
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al
Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Mg
B. Ca
C. Fe
D. Al
Hòa tan hết 3,24 gam kim loại M trong dung dịch H2SO4 loãng dư, thấy thoát ra 4,032 lít khí H2 (đktc). Kim loại M là
A. Al.
B. Fe
C. Na
D. Mg
Cho 6g một hỗn hợp A gồm hai kim loại sắt vả đồng hòa tan vào 500ml dung dịch HCl 2M dư, thu được V1 lít khí H2 (đktc), dung dịch B và 3,2 gam chất rắn. Cho 6g một hỗn hợp A tác dụng với dung dịch H2SO4 đặc nóng dư thu được V2 lít khí (đktc).
a) Tính khối lượng sắt và đồng trong hỗn hợp A. Tính V1 và V2
b) Tính C% các chất trong dung dịch B coi thể tích dung dịch thay đổi không đáng kể
Bài 24*: Khử hoàn toàn m gam một oxit sắt cần dùng 5,376 lít khí H2 (đktc), thu lấy kim loại sắt sinh ra cho tác dụng với dung dịch HCl dư thì thấy thoát ra 4,032 lít H2 (đktc). Tìm công thức hóa học của oxit sắt và tính giá trị m. Biết phản ứng của Fe với dung dịch HCl tạo ra muối sắt (II).
\(CT:Fe_xO_y\)
\(Fe_xO_y+yH_2\underrightarrow{^{t^o}}xFe+yH_2O\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\)
\(n_{Fe}=n_{H_2\left(2\right)}=\dfrac{4.032}{22.4}=0.18\left(mol\right)\)
\(n_{H_2\left(1\right)}=\dfrac{y}{x}\cdot n_{Fe}=\dfrac{5.376}{22.4}=0.24\left(mol\right)\)
\(\Leftrightarrow\dfrac{y}{x}\cdot0.18=0.24\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)
\(m_{Fe_3O_4}=\dfrac{0.18}{3}\cdot232=13.92\left(g\right)\)
Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). M là
A. Mg
B. Ca
C. Fe
D. Al
Câu 9: Cho 16,2 gam kim loại M, hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCl dư thấy bay ra 13,44 lít H2 ở đktc. Kim loại M là?
\(n_{H_2}=\dfrac{13.44}{22.4}=0.6\left(mol\right)\)
\(n_{M\left(pu\right)}=a\left(mol\right)\)
Bảo toàn e :
\(na=0.15\cdot4+0.6\cdot2=1.8\)
\(a=\dfrac{1.8}{n}\)
\(M=\dfrac{16.2}{\dfrac{1.8}{n}}=9n\)
\(n=3\Rightarrow M=27.M:Al\)
Bảo toàn e toàn bộ quá trình ta có: $n_{M}=\frac{1,8}{n}(mol)$
$\Rightarrow M_{M}=9n$
Lập bảng biện luận suy ra M là Al